Un atom este cea mai mică unitate constitutivă a materiei comune care are proprietățile unui element chimic. Conform ipotezei De Broglie, atomii sunt suficient de mici încât încercarea de a le prezice comportamentul folosind fizica clasică - de exemplu, ca și cum ar fi niște bile de biliard - dă predicții vizibil incorecte din cauza efectelor cuantice.
Fiecare atom este format dintr-un nucleu și din unul sau mai mulți electroni legați de nucleu. Nucleul este format din unul sau mai mulți protoni și, de obicei, dintr-un număr similar de neutroni. Protonii și neutronii se numesc nucleoni. Peste 99,94% din masa unui atom este concentrată în nucleu.
Proprietățile particulelor subatomice
Protonii au sarcină electrică pozitivă, electronii au sarcină electrică negativă, iar neutronii nu au sarcină electrică. Dacă numărul de protoni este egal cu cel de electroni, atunci atomul este neutru din punct de vedere electric. Electronii unui atom sunt atrași de protonii din nucleul atomic de această forță electromagnetică.
Protonii și neutronii din nucleu sunt atrași unul de celălalt printr-o altă forță, forța nucleară, care de obicei este mai puternică decât forța electromagnetică de respingere ce acționează între protonii încărcați pozitiv.
Masa și sarcina particulelor
- Electronul: este de departe cel mai puțin masiv dintre particulele constituente ale atomului, având o masă de 9,11×10⁻³¹ kg și o sarcină electrică negativă. Este cea mai ușoară particulă cu masă de repaus pozitivă măsurată. Masa electronului este de aproximativ 2000 de ori mai mică decât masa protonului.
- Protonul: are o sarcină pozitivă și o masă de 1,6726×10⁻²⁷ kg, fiind de 1836 de ori mai mare decât cea a electronului.
- Neutronul: nu are sarcină electrică și are o masă liberă de 1,6749×10⁻²⁷ kg, fiind cea mai grea dintre cele trei particule constituente, dar el poate fi redus prin energia de legătură nucleară. Masa sa este aproximativ egală cu masa protonului.
În condiții normale, electronii sunt legați de nucleul încărcat pozitiv prin atracția creată între sarcinile electrice de semn opus. Dacă un atom are mai mulți sau mai puțini electroni decât numărul său atomic, atunci el devine încărcat negativ sau, respectiv, pozitiv în ansamblu; un atom încărcat electric se numește ion.
Identificarea elementelor și izotopilor
Numărul de protoni din nucleu definește elementul chimic căruia îi aparține atomul. Numărul de neutroni definește izotopul elementului. Numărul de electroni influențează proprietățile magnetice ale unui atom.
Atomii aceluiași element au același număr de protoni, numit număr atomic (Z). Într-un singur element, numărul de neutroni poate varia, determinând izotopii acelui element. Numărul total de protoni și neutroni determină nuclidul.
Tabelul periodic
Există un instrument foarte util, numit tabelul periodic, în care elementele sunt organizate în funcție de structura atomică și, în consecință, de proprietățile lor. Elementele care stau la baza a tot ceea ce există nu sunt produse în mod sintetic, ci se pot găsi în natură.
Evoluția înțelegerii atomului
Ideea că materia este alcătuită din unități discrete este o idee foarte veche, care apare în multe culturi antice, cum ar fi Grecia și India. Cuvântul „atom” a fost inventat de vechii filosofi greci. Cu toate acestea, aceste idei își aveau fundamentul mai mult în raționamentele filozofice și teologice, decât în dovezi și experimente.
De la filosofie la știință
La începutul anilor 1800, John Dalton a folosit conceptul de atomi pentru a explica de ce elementele reacționează întotdeauna în raporturi de numere întregi mici (legea proporțiilor multiple). Acest model comun în chimie i-a sugerat lui Dalton că elementele care reacționează în număr întreg multiplu de unități discrete - cu alte cuvinte, atomi.
În 1827, botanistul Robert Brown a observat fenomenul cunoscut sub numele de „mișcare browniană”, considerat a fi cauzat de ciocnirea granulelor de praf de către moleculele de apă.
Descoperirea electronului și a nucleului
Fizicianul J. J. Thomson a măsurat masa razelor catodice, arătând că ele sunt formate din particule, dar că acestea sunt de circa 1800 de ori mai ușoare decât cel mai ușor atom, cel de hidrogen. Acestea au fost denumite electroni, prima particulă subatomică descoperită. Thomson a primit în 1906 Premiul Nobel în Fizică pentru acest lucru, răsturnând credința că atomii sunt particulele finale, indivizibile, de materie.
În 1909, Hans Geiger și Ernest Marsden, sub conducerea lui Ernest Rutherford, au bombardat o folie metalică cu particule alfa. Ei au constatat că unele particule alfa sunt deviate la unghiuri mai mari de 90°, ceea ce a dus la concluzia lui Rutherford că atomii au un mic volum în centru unde se găsesc sarcinile pozitive (nucleul) și că atomul este format în mare parte din spațiu gol.
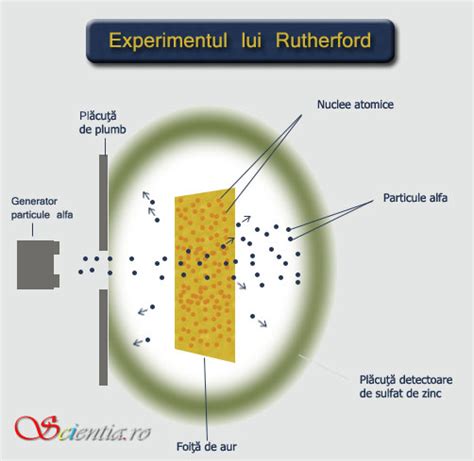
Dezvoltarea modelelor atomice
Modelul lui Rutherford consta dintr-o minge foarte mică în care se găsește sarcina pozitivă și se află în central atomului, minge pe care a numit-o nucleu și pentru a asigura neutralitatea atomului, din electronii care au sarcini negative și se invart în jurul nucleului, întregul sistem fiind asemănător cu sistemul planetar.
Modelul Bohr al atomului a introdus ideea că electronii fac „salturi cuantice” instantanee de la o orbită la alta. Mai târziu, Henry Moseley a furnizat noi dovezi experimentale în favoarea teoriei lui Niels Bohr, rafinând modelele lui Ernest Rutherford și Antonius van den Broek.
Fizica nucleară și particulele elementare
Oamenii de știință care activează în domeniul fizicii nucleare cercetează caracteristicile nucleelor atomice. Protonii și neutronii s-au dovedit a fi hadroni, adică compuși din particule mai mici numite quarkuri.
În Modelul Standard al fizicii, electronii sunt considerați particule elementare, fără structură internă. Cu toate acestea, atât protonii, cât și neutronii sunt particule compozite alcătuite din quarkuri. Protonii sunt compuși din două quarkuri up și un quark down, iar neutronii constau dintr-un quark up și două quarkuri down. Quarkurile sunt ținute împreună de interacțiunea tare (sau forța nucleară tare), care este mediată de gluoni.
Forțele fundamentale
Protonii și neutronii sunt ținuți unul lângă altul în nucleu de forța nucleară, care este un reziduu al unei forțe tari cu proprietăți oarecum diferite în raport cu raza de acțiune. Aceasta este una dintre cele patru tipuri de forte fundamentale din Univers.
Fuziunea și fisiunea nucleară
Fuziunea nucleară apare atunci când mai multe particule atomice se unesc pentru a forma un nucleu mai greu. De exemplu, în centrul Soarelui, protonii necesită energii de 3-10 keV pentru a depăși respingerea și a fuziona într-un singur nucleu.
Fisiunea nucleară este procesul invers, provocând divizarea unui nucleu în două nuclee mai mici. Dacă în urma unei reacții de fuziune masa nucleului este mai mică decât suma maselor particulelor separate, atunci diferența dintre aceste două valori poate fi emisă sub forma unui tip de energie utilizabilă, așa cum descrie formula lui Albert Einstein a echivalenței masă-energie E = mc².
Fizică; cl. IX, "Fisiunea nucleelor de uraniu. Energetică atomică nucleară"
Compoziția materiei
Știm astăzi că toate corpurile pe care le observăm în mediul înconjurător sunt combinații diferite ale unor elemente. Elementul, în concepția modernă, conține doar un anumit fel de materie. Totul în mediul înconjurător este alcătuit din elemente.
Sunt substanțe care reprezintă amestecuri de elemente (de ex. aerul) sau amestecuri de compuși chimici. Doi, trei sau mai mulți atomi se pot grupa și legăturile dintre ei sunt atât de puternice încât este foarte dificil să fie separați. O astfel de grupare strânsă a atomilor reprezintă o moleculă. Molecula este cea mai mică particulă a unei substanțe capabilă să aibă o existență stabilă.
Originea elementelor
Elementele mai ușoare decât fierul sunt produse într-un proces numit nucleosinteză, care are loc în interiorul stelelor. Elementele mai grele se formează atunci când stelele mor în explozii uriașe numite supernove.

tags: #care #dintre #elementele #prezentate #are #cea