Stabilirea formulei structurale a unei substanțe se poate face urmând o schemă bine definită, care implică mai mulți pași esențiali. Această metodologie permite înțelegerea profundă a modului în care atomii sunt legați între ei într-o moleculă și a distribuției sarcinilor electrice.
Etapele stabilirii formulei structurale
Procesul de determinare a formulei structurale începe cu identificarea tipului de legături chimice prezente în moleculă. Ulterior, se explorează diverse posibilități de aranjare a atomilor și se aplică criterii pentru a selecta structura corectă. În final, se verifică respectarea regulilor de valență prin distribuirea electronilor.
-
Identificarea tipurilor de legături: Primul pas constă în a stabili care dintre legăturile din cadrul moleculei sunt ionice și care sunt covalente. Această distincție este fundamentală pentru înțelegerea comportamentului chimic al substanței.
-
Scrierea formulelor de schelet: Apoi, se scriu formulele de schelet ale compusului în toate formele posibile. Acestea reprezintă aranjamentele preliminare ale atomilor, fără a lua încă în considerare electronii.
-
Alegerea formulei valabile: Pe baza unor criterii fizice sau chimice ajutătoare, se apreciază care dintre formulele de schelet propuse sunt valabile. Această etapă implică adesea utilizarea datelor experimentale sau a unor principii chimice stabilite.
-
Distribuirea electronilor de valență: Se insumează electronii de valență ai tuturor atomilor și se plasează în cadrul scheletului astfel încât să se respecte regula octetului pentru fiecare atom. Această regulă stipulează că atomii tind să obțină o configurație electronică stabilă, similară celei a gazelor nobile, prin formarea de legături.
-
Calcularea sarcinii formale: În final, se determină sarcina formală (respectiv sensul covalențelor dative) prin scăderea din numărul electronilor de valență ai elementului respectiv, a electronilor implicați în formarea legăturilor. Sarcina formală ajută la înțelegerea distribuției sarcinilor electrice în cadrul moleculei.
Exemplu: Apa oxigenată (H₂O₂)
Pentru a ilustra procesul, să analizăm cazul apei oxigenate (H₂O₂).
-
În molecula de apă oxigenată, toate legăturile sunt covalente.
-
Formulele de schelet posibile sunt:
- a) H-O-O-H
- b) HOOH
- c) HOO a (unde "a" ar fi un alt atom, ipotetic)
-
Formula a) nu este corectă deoarece hidrogenul este monovalent, iar măsurătorile fizice confirmă că molecula de H₂O₂ este simetrică. Formula c) nu este relevantă pentru compoziția H₂O₂. Prin urmare, varianta corectă este doar b) HOOH.
-
Numărul total de electroni de valență pentru H₂O₂ este 1 (de la primul H) + 6 (de la primul O) + 6 (de la al doilea O) + 1 (de la al doilea H) = 14 electroni, adică 7 perechi de electroni. Plasarea acestor electroni, respectând regula octetului, conduce la structura: H-O-O-H, unde fiecare atom de oxigen este legat de hidrogen și de celălalt atom de oxigen, iar atomii de oxigen au și perechi de electroni neparticipanți.
-
Calculul sarcinilor formale confirmă neutralitatea moleculei, cu sarcini formale de 0 pentru fiecare atom.
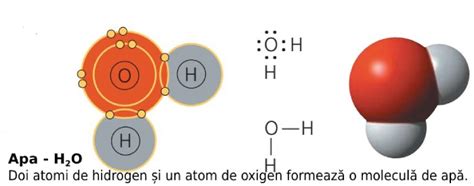
Istoricul conceptului de moleculă
Conceptul de moleculă, ca unitate fundamentală a materiei, are rădăcini adânci în istoria gândirii umane. Filozofi greci antici, precum Leucip și Democrit, au postulat existența atomilor ca fiind elementele constitutive ale universului. Mai târziu, în secolul al XVII-lea, Robert Boyle, în lucrarea sa "The Sceptical Chymist", a sugerat că materia este compusă din grupuri de particule, iar schimbările chimice rezultă din rearanjarea acestora. El a numit aceste particule de bază "corpuscule".
În secolul al XVIII-lea, William Higgins a publicat idei despre "combinații de particule ultime", prefigurând conceptul de legături de valență. Investigațiile moderne asupra naturii moleculelor și a legăturilor dintre ele au început să prindă contur în secolul al XVII-lea și au evoluat semnificativ odată cu apariția fizicii cuantice.
Un moment crucial a fost în 1926, când fizicianul francez Jean Perrin a primit Premiul Nobel pentru Fizică pentru demonstrarea existenței moleculelor prin calcularea constantei Avogadro prin trei metode diferite. Ulterior, în 1927, fizicienii Fritz London și Walter Heitler au aplicat mecanica cuantică pentru a explica legăturile din molecula de hidrogen, un studiu considerat un punct de referință în aplicarea mecanicii cuantice în chimie.
În 1931, Linus Pauling, bazându-se pe aceste lucrări, a publicat articolul său revoluționar "The Nature of the Chemical Bond", în care a folosit mecanica cuantică pentru a calcula proprietățile și structurile moleculare. El a dezvoltat teoria hibridizării, esențială pentru explicarea legăturilor în molecule precum metanul (CH₄).
Definiția și proprietățile moleculelor
În teoria cinetică a gazelor, termenul "moleculă" este adesea utilizat pentru orice particulă gazoasă, indiferent de compoziția sa. Definiția modernă a moleculei, în științele moleculare, se referă la un sistem stabil (stare legată) compus din doi sau mai mulți atomi. Ionii poliatomici pot fi considerați, în anumite contexte, molecule încărcate electric.
Moleculele sunt omniprezente în natură, alcătuind majoritatea substanțelor organice, inclusiv cele esențiale vieții, precum proteinele, acizii nucleici (ADN și ARN), carbohidrații, grăsimile și vitaminele. Cu toate acestea, multe substanțe familiare, cum ar fi mineralele, sărurile și metalele, nu sunt alcătuite din molecule discrete, ci din structuri cristaline sau rețele ionice.
Moleculele sunt, în general, menținute împreună prin legături covalente, care implică partajarea perechilor de electroni între atomi. Legătura ionică, pe de altă parte, implică atracția electrostatică dintre ioni cu sarcini opuse și este caracteristică compușilor ionici.
Dimensiunile moleculelor variază considerabil. Majoritatea moleculelor sunt prea mici pentru a fi văzute cu ochiul liber, având dimensiuni de ordinul angstromilor (aproximativ o miliardime de metru). Totuși, moleculele multor polimeri, inclusiv biopolimeri precum ADN-ul, pot atinge dimensiuni macroscopice.
Formula chimică a unei molecule utilizează simboluri ale elementelor, numere și alte notații pentru a reprezenta compoziția sa. Există diverse tipuri de formule, inclusiv:
- Formula empirică: Reprezintă cel mai simplu raport de numere întregi al elementelor chimice dintr-un compus.
- Formula moleculară: Indică numărul exact de atomi care compun molecula.
Moleculele cu aceeași formulă moleculară, dar cu aranjamente atomice diferite, se numesc izomeri. Aceștia pot avea proprietăți fizice și chimice distincte.
Spectroscopia moleculară și determinarea structurii
Spectroscopia moleculară este un domeniu esențial în studiul moleculelor, deoarece analizează răspunsul acestora la interacțiunea cu diverse tipuri de radiații electromagnetice. Prin analiza spectrelor obținute, se pot determina informații detaliate despre structura, legăturile și chiar compoziția moleculelor.
- Spectroscopia în microunde: Măsoară modificările în rotația moleculelor și este utilizată, printre altele, pentru identificarea moleculelor în spațiul cosmic.
- Spectroscopia în infraroșu: Analizează vibrațiile moleculelor (întindere, îndoire, răsucire) și este utilă pentru identificarea tipurilor de legături și a grupurilor funcționale.
- Spectroscopia UV-Vis: Studiază modificările în aranjamentele electronilor, care duc la absorbția sau emisia de lumină în regiunea ultravioletă și vizibilă, fiind responsabilă pentru culoarea substanțelor.
Studiul moleculelor prin fizica moleculară și chimia teoretică se bazează pe principiile mecanicii cuantice și este fundamental pentru înțelegerea legăturii chimice. Cea mai simplă moleculă cunoscută este ionul molecular de hidrogen (H₂⁺), unde legătura este formată dintr-un singur electron.
Spectre de linii de emisie și absorbție - Fizică de nivel avansat
Definiția riguroasă a unei molecule, propusă de IUPAC, implică existența unei depresiuni pe suprafața de energie potențială, suficient de adâncă pentru a limita cel puțin o stare vibrațională. Această definiție se concentrează pe stabilitatea interacțiunii dintre atomi, indiferent de natura acesteia.
tags: #sarcina #formala #a #molweculelor