Proiectul vizează implementarea, la nivel de laborator și unitate pilot, a unei abordări integrate pentru producția de formule vaccinale inovatoare, menite să sporească capacitatea de răspuns rapid la provocările de sănătate publică. Soluțiile propuse se concentrează pe obținerea de antigene proteice prin tehnologia ADN recombinant, utilizând atât sisteme procariote (tulpini E. coli), cât și sisteme eucariote (linii celulare HEK293, celule de insecte) ca platforme de sinteză.
Proteinele obținute sunt ulterior condiționate sub formă de ansambluri nanoparticulate, fie prin utilizarea unor „triggeri” de auto-asamblare, fie prin sisteme de adjuvanți de tip „oil-in-water”. Întregul proces va fi supus unui mecanism de optimizare continuă, adresându-se fiecărei etape specifice. Optimizările vor viza design-ul secvențelor ADN codificatoare, vectorii utilizați, condițiile de cultură pentru expresie proteică crescută, metodele de purificare, calitatea structurală și variantele de asamblare și adjuvantare a antigenelor.
Rezultatele principale preconizate constau în preparate vaccinale cu eficiență dovedită la nivel de studiu pe model de animal de laborator, a căror producție este fezabilă la nivel de unitate pilot. Ca rezultat secundar, se va dezvolta un „pipeline” bicomponent care va cuprinde producția de antigene cu potențial vaccinal și asamblarea acestora sub formă de nanostructuri, cu sau fără adjuvant. Acest livrabil are o valoare potențială intrinsecă mai mare, oferind flexibilitate și reacție rapidă în situații de urgență medicală la nivel regional.
Contextul Dezvoltării Vaccinurilor
Dezvoltarea vaccinurilor reprezintă o prioritate globală pentru combaterea afecțiunilor cauzate de agenții infecțioși, vaccinarea fiind considerată cea mai eficientă soluție. Tradițional, vaccinurile sunt produse prin tehnologii bazate pe patogeni inactivați sau atenuați, care necesită propagare pe culturi celulare sau ouă embrionate.
În ultimii ani, pandemia cauzată de SARS-CoV-2 a stimulat dezvoltarea de noi tehnologii, cele mai de succes abordări fiind cele care au permis producție rapidă, precum vaccinurile bazate pe ARN mesager. Deși sistemul ARN mesager și „carrier”-ul lipidic este teoretic adaptabil la orice secvență de antigen, dezvoltarea acestor vaccinuri este costisitoare și necesită optimizări intensive. Investițiile enorme necesare pentru vaccinurile anti-SARS-CoV-2, deși accesibile marilor consorții farmaceutice private, sunt prohibitive pentru instituțiile de sănătate publică. În plus, aceste vaccinuri au generat reticență publică, asociată cu măsurile restrictive impuse în pandemie.
Prin urmare, capacitatea globală de dezvoltare rapidă de vaccinuri pentru uz uman la costuri reduse nu este o noutate, ci, mai degrabă, o raritate. Infecțiile respiratorii virale, precum cele cauzate de SARS-CoV-2, virusul respirator sincițial (RSV) sau virusul gripal, pot crea dezastre la nivel mondial, cauzând deteriorarea rapidă a stării de sănătate, complicații grave și rate ridicate de mortalitate.
Abordări Vaccinale pentru SARS-CoV-2 și Alte Virusuri Respiratorii
Vaccinurile SARS-CoV-2 sunt investigate în numeroase studii clinice, cu accent pe obținerea unor titruri ridicate de anticorpi neutralizanți anti-proteina S. Multiple vaccinuri bazate pe proteina S sau pe domeniul de legare la receptor (RBD) sunt în studii clinice, inclusiv proteine S trimerice recombinante, domenii RBD monomerice sau trimerice, livrate prin vectori virali sau ARNm. Cu toate acestea, nu este clar care dintre aceste ținte vaccinale oferă un potențial superior în ceea ce privește imunogenitatea sau capacitatea neutralizantă. Date recente sugerează că vaccinurile pe bază de proteine recombinante ar putea completa vaccinurile pe bază de acizi nucleici sau cu vectori virali. În prezent, peste 10 candidați vaccinali pe bază de proteine recombinante sunt evaluați în studii clinice, iar peste 50 în studii preclinice, în combinație cu diverși adjuvanți pentru creșterea imunogenicității.
Virusul sincițial respirator (RSV) este principala cauză de infecții de tract respirator inferior la sugari, vârstnici și adulți imunodeprimați. În prezent, nu există un vaccin autorizat pentru prevenirea infecțiilor provocate de RSV. Dezvoltarea vaccinurilor anti-RSV a întâmpinat dificultăți, inclusiv cazul vaccinului pe bază de RSV inactivat cu formol, care a determinat exacerbarea bolii respiratorii prin polarizarea răspunsului imun spre un răspuns de tip Th2 și producerea de anticorpi cu eficacitate scăzută. Există un interes crescut pentru dezvoltarea unor vaccinuri subunitare sigure și cu specificitate crescută, în special vizând proteina de fuziune F, a cărei administrare s-a dovedit sigură și eficientă în studii clinice. Conformația proteinei F pre-fuziune este preferabilă celei post-fuziune datorită inducerii de anticorpi neutralizanți.
Epidemia de gripă reprezintă o amenințare anuală, din cauza lipsei unui vaccin care să ofere protecție încrucișată împotriva virusurilor gripale noi și emergente. Se depun eforturi pentru dezvoltarea unui vaccin universal, o strategie atractivă fiind combinarea antigenelor conservate care induc protecție încrucișată mediată de anticorpi cu epitopi care induc protecție încrucișată mediată de limfocite T.
Dezavantajele Vaccinurilor Tradiționale pe Bază de Ouă Embrionate
În ceea ce privește vaccinurile antigripale tradiționale pe bază de ouă embrionate, deși pot proteja împotriva infecției, există eforturi semnificative pentru dezvoltarea de platforme alternative menite să depășească dezavantajele existente. Printre acestea se numără dificultatea aprovizionării cu ouă embrionate în context pandemic, etapele lungi de producție și dependența de adaptarea izolatelor umane de virus pentru propagarea pe ouă embrionate. De asemenea, adaptarea virusului gripal pe ouă poate determina substituția unor aminoacizi în structura hemaglutininei (HA), ceea ce poate duce la alterarea sau eliminarea situsurilor antigenice dominante.
Inovația în Producția de Biofarmaceutice
În ultimii ani, s-a observat că instituțiile publice întâmpină dificultăți în a concura cu marile corporații farmaceutice în ceea ce privește inovația și producția de biofarmaceutice. Deși acest fapt este considerat normal în filozofia pieței libere, în situații de criză de sănătate publică, statul are datoria de a asigura protecția cetățenilor. În contextul pandemiei SARS-CoV-2, stocurile limitate de vaccinuri și regulile pieței libere au împiedicat multe state să furnizeze suficiente doze de vaccin propriilor cetățeni.
România, prin apartenența la Uniunea Europeană, a beneficiat de doze de vaccin, dar în situații viitoare, în funcție de infecțiozitatea patogenului, gravitatea simptomelor sau dificultatea generării unui tratament, există riscul de a nu se putea asigura protecția populației.
Abordarea „Outside the Box” a Proiectului
Unul dintre principiile definitorii ale proiectului este „outside the box thinking”. Deoarece nu este realistă competiția cu entitățile private în ceea ce privește tehnologiile de dezvoltare de vaccin, proiectul propune explorarea unor soluții în zone mai puțin populare. Una dintre acestea vizează vaccinurile bazate pe proteine recombinante, o tehnologie eclipsată de succesele recente ale vaccinurilor de tip ARN mesager.
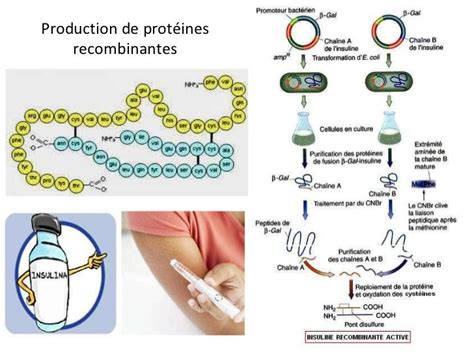
Pentru a explora o zonă și mai puțin populară, proiectul își propune sinteza de proteine recombinante în sistem procariot. Există literatură științifică abundentă care tratează aplicațiile proteinelor sintetizate în E. coli. Similar cu tehnologia ARN mesager, odată cunoscut genomul patogenului, se poate sintetiza în laborator secvența de nucleotide corespunzătoare proteinei de interes.
Procesul de Sinteză a Proteinelor Recombinante în E. coli
Sinteza proteinelor recombinante se realizează, de regulă, prin tehnici de inginerie genetică, cum ar fi Overlap Extension PCR (OE-PCR), utilizând primeri de dimensiuni mari cu capete complementare care acoperă întreaga secvență a genei. În această etapă, secvența nucleotidică poate fi optimizată prin utilizarea preponderentă a codonilor specifici sistemului de expresie.
După obținerea secvenței codificatoare, aceasta poate fi inserată, prin clonare mediată de restricție enzimatică și ligare, într-un vector plasmidial. Plasmidul astfel obținut conține, pe lângă gena de interes, o secvență promoter (ex. T7) în amonte, care asigură abundența transcripției, o secvență pentru selecția pe baza rezistenței la un antibiotic și o origine a replicării pentru multiplicare.
Ulterior, plasmidul este inserat în bacterii (de regulă, tulpini E. coli) prin transformare bacteriană sau electroporare. Bacteriile sunt crescute în mediu cu antibiotic de selecție și, sub influența unui inductor, declanșează producția de proteină. În condiții optime, la nivel de laborator, producția de proteină durează 3-5 ore și generează sute de miligrame de proteină de interes per litru. Având în vedere că o doză de vaccin gripal produs prin mijloace tradiționale conține aproximativ 15µg, teoretic, prin sinteză în bacterii, se pot genera echivalentul a peste 10.000 de doze pe litru într-un timp foarte scurt, cu costuri minime.
Pentru îmbunătățirea randamentului, creșterea culturilor bacteriene și capacitatea de sinteză pot fi optimizate. După liza bacteriană, proteina de interes este eliberată în mediul extracelular și poate fi purificată prin mijloace cromatografice, precum cromatografia de afinitate, de excluziune sterică (SEC) și de schimb ionic (IEX). În plus, impurități de tipul LPS pot fi îndepărtate prin IEX sau cu rășini cu afinitate pentru LPS.
În scopul expresiei de proteine cu randament ridicat și pentru a facilita purificarea proteinelor recombinante, se vor produce și variante proteice fuzionate cu „elastin-like polypeptides” (ELP). Acestea, prin tranziția de faze, formează aglomerări ordonate, de dimensiuni nanometrice, utilizate ca nanoparticule autoasamblabile.
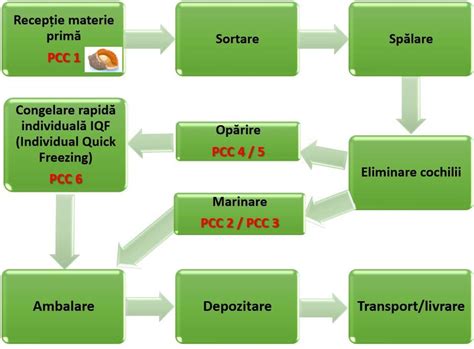
Optimizarea Expresiei și Purificării Proteinelor
Procesul de optimizare a expresiei și purificării proteinelor implică mai multe etape:
- Designul ADN: Se va realiza design-ul in silico al secvențelor ADN, optimizând codoni, utilizând secvențe linker, inserând situsuri pentru enzime de restricție, realizând proteine de fuziune și cuplând cu secvențe care promovează nanostructurarea. Vor fi folosite tehnici clasice de inginerie genetică, cum ar fi PCR și variațiuni de tipul Heterostagger-PCR, Overlap-Extension PCR.
- Construcția Vectorilor: Se vor alege cei mai potriviți vectori plasmidiali, ținând cont de sistemul de expresie (procariot sau eucariot). Această activitate va reuni rezultatele celor două activități anterioare și va consta în prepararea constructelor de tip vector - secvență codificatoare, utilizând clonare prin restricție cu enzime de restricție, clonare TA sau clonare fără ligare.
- Expresia Proteică: Se va realiza un studiu privind cele mai potrivite tulpini E. coli pentru expresie procariotă și cele mai potrivite linii celulare mamaliene/de insecte pentru expresie în sistem eucariot. Vor fi testate mai multe tipuri de medii de cultură pentru sistemele de expresie a proteinelor. Parametrii de cultură vor fi corelați cu markeri transcriptomici pentru a permite modificări informate și obținerea unui randament crescut.
- Extracția, Purificarea și Refoldarea: Se vor utiliza parametrii de cultură descriși anterior pentru expresia proteinelor de interes. Pentru fiecare proteină, se va aborda o strategie specifică de extracție, purificare și, după caz, refoldare. Extracția se va realiza prin liză prin ultrasunete, tratament cu detergenți sau alte metode adecvate.
Formularea și Adjuvantarea Antigenelor
Antigenele purificate sunt, în general, slab imunogene, motiv pentru care alegerea adjuvanților și a sistemelor de livrare a vaccinului este crucială pentru creșterea imunogenității și favorizarea unui răspuns imun protector. Adjuvanții și modalitatea de formulare pot influența considerabil calitatea răspunsului imun umoral/celular indus de vaccin.
În cazul nanoparticulelor autoasamblabile, se va folosi sistemul bazat pe ELP. De asemenea, se vor explora alte abordări pentru inducerea autoasamblării, cum ar fi cuplarea cu feritină sau inducerea de mutații care promovează multimerizarea.

Evaluarea Imunogenității Candidaților Vaccinali
Inițierea răspunsului imun față de un antigen debutează cu activarea celulelor imune înnăscute, în special a celulelor dendritice (DC), care sunt cele mai eficiente celule prezentatoare de antigen și joacă un rol esențial în inducerea și orientarea răspunsului imun adaptativ.
După captarea antigenului, DC suferă procesul de maturare și migrează în organele limfoide adiacente, unde activează limfocitele T CD4+. Citokinele secretate de DC direcționează diferențierea limfocitelor T CD4+ în subseturi distincte (Th1, Th2), care, la rândul lor, influențează calitatea răspunsului imun umoral mediat de anticorpi.
În cadrul proiectului, se va evalua capacitatea candidaților vaccinali de a induce maturarea DC și activarea limfocitelor T într-un model in vitro de cocultură DC-limfocite T. Candidații vaccinali cu potențial imunogen vor fi selectați și, în urma imunizării animalelor de laborator, se va evalua efectul vaccinării asupra polarizării răspunsului imun adaptativ.
Exemple de Vaccinuri și Platforme Vaccinale
Efluelda este un vaccin antigripal destinat persoanelor cu vârsta de 60 de ani și peste, oferind protecție împotriva celor trei tulpini de virus gripal conținute în vaccin, aproximativ 2-3 săptămâni după administrare. Gripa este o afecțiune respiratorie contagioasă, cauzată de virusuri gripale, care poate varia de la ușoară la severă, cu complicații grave, precum pneumonia, putând duce la spitalizare sau deces. Vaccinarea anuală este recomandată din cauza schimbării anuale a tulpinilor virale circulante și a duratei protecției.
Vaccinul împotriva rujeolei este un vaccin viu hiperatenuat, utilizat pentru prevenirea rujeolei la copii, începând cu vârsta de 12 luni. În anumite condiții (copii din colectivități, țări cu incidență crescută a rujeolei), vaccinarea poate începe de la 9 luni, cu rapel la 6 luni, putând fi asociat cu vaccinarea antiurliană și antirubeolică. Administrarea se poate face intramuscular sau subcutanat.
Vaccinul ROMPORPOX este destinat imunizării active a porumbeilor împotriva variolei aviare. Acesta este un vaccin liofilizat, administrat prin badijonarea pielii deplumate de pe fața laterală a gambei, la porumbeii cu vârsta de peste 5 săptămâni. Nu produce reacții generale postvaccinale.
Vaccinul ROKOVAC NEO este un vaccin veterinar administrat intramuscular pentru imunizarea activă a porcinelor împotriva rotavirozei și colibacilozei. Antigenele din vaccin activează sistemul imunitar și producerea de anticorpi. Preparatul conține uleiuri minerale, iar injectarea accidentală poate cauza edeme intensive, necroză ischemică sau chiar pierderea degetului.
Vaccinul pentru boala Marek este destinat imunizării active a ouălor embrionate de 18 zile de găină sau a puilor de găină de o zi, pentru reducerea mortalității, semnelor clinice și leziunilor cauzate de tulpinile blânde și virulente ale virusului bolii Marek. Administrarea se face in-ovo (0,05 ml per ou) sau subcutanat (0,2 ml per pui la o zi vechime). Imunitatea se instalează în 9 zile post-vaccinare și durează pe perioada riscului.

Reacții adverse generale și precauții: Unele vaccinuri pot cauza reacții adverse precum febră, simptome respiratorii tranzitorii, exantem ușor, convulsii hipertermice (rar), purpură trombocitopenică (rar). Este importantă informarea medicului sau farmacistului cu privire la orice reacție adversă.
Contraindicații: Sarcina (pentru anumite vaccinuri), imunodepresia congenitală sau dobândită, administrarea recentă de imunoglobuline, alergia cunoscută la neomicină sau la proteine de ou (pentru vaccinurile preparate pe culturi de celule embrionate de pui). În cazul copiilor născuți din mame HIV pozitive, statusul serologic nu poate fi stabilit până la vârsta de 9-10 luni.
Condiții de păstrare: Vaccinurile trebuie păstrate la frigider (2°C - 8°C) și nu trebuie congelate. Nu trebuie aruncate în mediul înconjurător.
Cum funcționează vaccinurile?
tags: #preparat #vaccinal #pe #oua #embrionate